ダイオキシンの毒性発現は芳香族炭化水素受容体(AhR)により媒介されることがノックアウトマウスの研究などにより明になってきました。AhRは通常細胞質にHsp90、p23、XAP2との複合体として存在し、ダイオキシンなどが結合すると核内に移行します。核内でHSP90複合体から解離してArntとヘテロ2量体を形成し、標的遺伝子のプロモーター領域の応答配列XREに結合して転写を活性化します。生体異物の酸素付加反応を触媒するCYP1A1は代表的な標的遺伝子として知られています。
AhRリプレッサー(AhRR)はその名が示すように、マウス細胞でAhRによるCYP1A1誘導の抑制因子として見出されました。そのメカニズムは(i)AhRとのArntの奪い合い、(ii)AhR/ArntとAhRR/Arnt両ヘテロダイマーのXRE配列への結合の拮抗に基づくことが明らかにされています。外来異物を認識する細胞内受容体型転写因子であるAhRは、標的遺伝子の転写活性化以外にも、細胞増殖や分化など様々な生理機能に影響を及ぼし、この生理機能のかく乱がダイオキシンなどの毒性発現のメカニズムとされている。AhRRはAhRの標的遺伝子であり、活性化されたAhRのオーバーランに対するネガティブフィードバックループを形成しているものと考えられています。
本研究室では、ラットを用いてAhRRの役割をin vivoで検討し、異物代謝の中心をなし、AhR高発現臓器である肝臓ではAhRRの構成および誘導発現レベルは他の臓器と比べて必ずしも高くないことから、細胞レベルで得られたAhRの転写活性化能に対する抑制的調節機能は、生体内では必ずしも重要ではないと考えています。これまで、AhRに対するドミナントネガティブ因子としての機能に注目が集中したため、AhRRの生理的機能についての報告は皆無です。本研究室では、AhRRのAhRに対するドミナントネガティブ因子としての機能以外の生理機能を明らかにすることを目的としています。
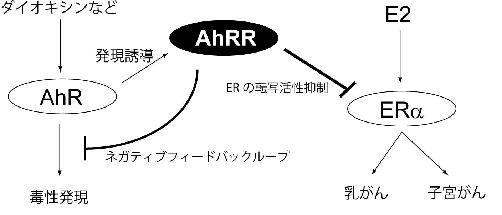
その一つとしてAhRRがステロイドホルモンレセプターの一つであるエストロゲンレセプターに結合し、それによる転写活性化を抑制することを明らかにしました(下図)。またAhRRを過剰発現するとエストロゲン依存的に増殖する乳がん細胞の増殖を抑制することがわかりました(下図)。