
MOMBhc-僋儘儘儂儖儊乕僩偺崌惉朄
![]()
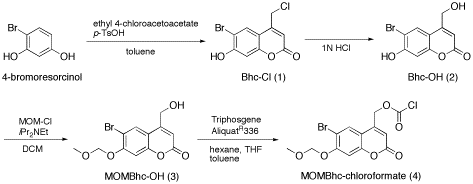
6-Bromo-4-chloromethyl-7-hydroxycoumarin (Bhc-Cl) (1)
100 mL僫僗宆僼儔僗僐偵丄僗僺僫乕丄Dean-Stark娗乮梕検5 mL偔傜偄乯丄娨棳椻媝婍乮嬍 晅偒乯偍傛傃墫壔僇儖僔僂儉娗傪庢傝晅偗偨丅4-bromoresorcinol傪1.9330 g (10.23 mmol)丄toluene 25 mL丄ethyl 4-chloroacetoacetate 2.0 mL (15.00 mmol)丄p-toluenesulfonic acid, monohydrate 225.0 mg (1.18 mmol)傪弴師壛偊丄偙偺梟塼傪潣漚偟側偑傜18帪娫150亷偱壛擬娨棳偟偨丅斀墳偑恑傓偲敄愒怓偺屌懱乮惗惉暔乯偑愅弌偟偰偔傞丅斀墳偺廔椆偼尨椏偺徚幐傪TLC偱妋擣偟偨丅斀墳廔椆屻丄斀墳梟塼傪幒壏偵栠偟丄toluene 2 mL丄忲棷悈25 mL傪壛偊偰昘忋偱奾漚偟偨丅偦偺拞偵偝傜偵n-Hexane 5 mL傪壛偊丄30暘奾漚偟偨丅惗惉偟偨捑揳傪媧堷鄅夁偟丄僨僔働乕僞乕撪偱姡憞偟偨丅搷怓暡枛偺栚揑暔傪1.4237 g (4.92 mmol, 48.0 %)偱摼偨丅
TLC (SiO2) 丂揥奐梟攠丗僕僋儘儘儊僞儞乛儊僞僲乕儖亖20乛1丄 Rf = 0.49
1H-NMR (270.05 MHz; CD3OD) 兟=4.80(2H, s) 6.42(1H, s) 6.85(1H, s) 7.95(1H, s)
6-Bromo-7-hydroxy-4-hydroxycoumarin (Bhc-OH) (2)
1 L僫僗宆僼儔僗僐偵丄僗僺僫乕丄娨棳椻媝婍乮嬍晅偒乯傪庢傝晅偗偨丅婎幙(1)傪1.1440 g (3.952 mmol)偲1N HCl傪300 mL壛偊偰丄140亷偱壛擬娨棳偟4.5擔奾漚偟偨丅斀墳偺廔椆偼尨椏偺徚幐傪TLC偱妋擣偟偨丅偦偺屻斀墳梟塼傪幒壏偵栠偟丄僄僶億儗乕僞乕偱梟攠傪彍嫀偟丄搷怓暡枛偺栚揑暔傪1.0359 g (3.822 mmol, 96.7%)偱摼偨丅偙偺斀墳偼僗働乕儖傾僢僾壜擻偱偁傞丅婎幙1 g偵懳偟丄1N HCl傪250 mL壛偊傞偺偑億僀儞僩丅
TLC (SiO2) 丂揥奐梟攠丗僕僋儘儘儊僞儞乛儊僞僲乕儖亖10乛1丄 Rf亖0.42
1H-NMR (270.05 MHz; CD3OD) 兟=4.77(2H, s) 6.38(1H, s) 6.84(1H, s) 7.81(1H, s) ; (DMSO-d6) 兟=4.70 (2H, d, J= 4.6 Hz), 5.63 (1H, t, J= 5.7 Hz), 6.27 (1H, s), 6.90 (1H, s), 7.84 (1H, s)
FT-IR (ATR) 兯= 3365, 3087, 1686, 1605, 1233, 1091, 1035, 925, 876, 847
UV (KMops) 兩max / nm (兠) : 365 nm (26500 M-1cm-1)
6-Bromo-7-methoxymethoxy-4-hydroxymethylcoumarin (MOMBhc-OH) (3)
50 mL僫僗宆僼儔僗僐偵丄僗僺僫乕丄墫壔僇儖僔僂儉娗傪庢傝晅偗偨丅婎幙(2)傪622.0 mg (2.295 mmol)丄扙悈DCM 6 mL丄chloromethyl methyl ether 226.6兪L (2.984 mmol)偲iPr2NEt 559.7兪L (3.213 mmol)傪弴師壛偊丄幒壏偱25暘奾漚偟偨丅斀墳偺廔椆偼尨椏偺徚幐傪TLC偱妋擣偟偨丅0.5 M僋僄儞巁傪壛偊傞偙偲偱斀墳傪掆巭偝偣丄僋儘儘儂儖儉偱拪弌偟偨丅偦偟偰丄桳婡憌傪MgSO4偱姡憞偝偣丄梟塼傪鄅夁偟偨丅梟攠傪尭埑彍嫀偡傞偙偲偱丄栚揑暔傪633.0 mg (2.008 mmol, 87.5%)摼偨丅
TLC (SiO2) 丂揥奐梟攠丗僕僋儘儘儊僞儞乛儊僞僲乕儖亖10乛1丄Rf亖0.56
1H-NMR (270.05 MHz; CDCl3) 兟= 1.93 (1H, t, J= 5.9 Hz), 3.52 (3H, s), 4.86 (2H, d, J=5.9 Hz), 5.32 (2H, s), 6.52 (1H, s), 7.16 (1H, s), 7.70 (1H, s)
13C-NMR (67.80 MHz; DMSO-d6) 兟= 56.23, 59.06, 94.80, 103.51, 107.49, 108.96, 112.75, 128.19, 153.51, 155.13, 155.76, 159.93
FT-IR (ATR) 兯= 3508, 1703, 1604, 1267, 1158, 1095, 1083, 1032, 1009, 974, 894, 842
6-Bromo-7-methoxymethoxycoumarin-4-ylmethoxycarbonyl chloride (MOMBhc-chloroformate) (4)
僩儕儂僗僎儞偐傜儂僗僎儞傪敪惗偝偣傞曽朄
亙昁梫側帋栻亜 丒 Triphosgene (Aldrich) 丒 AliquatR 336 (tricaprylylmethylammonium chloride) (Aldrich) 丒 扙悈僿僉僒儞乮儌儗僉儏儔乕僔乕僽4A偱姡憞乯乮榓岝弮栻乯 丒 扙悈僩儖僄儞乮儌儗僉儏儔乕僔乕僽4A偱姡憞乯乮榓岝弮栻乯 丒 扙悈THF (榓岝弮栻) 亙敪惗曽朄亜 僒儞僾儖價儞偵AliquatR 336傪136.5兪L (0.299 mmol)偼偐傝庢傝丄偦傟傪扙悈僿僉僒儞4 mL偱梟偐偡丅懴埑價儞(20 mL僒僀僘丄Hyperglasstor, THG-A2, TAIATSU Techno)偵僗僺僫乕傪擖傟丄偦偺屻Triphosgene傪1.513 g (5.101 mmol)擖傟丄僿僉僒儞偵梟夝偟偨AliquatR 336傪壛偊傞丅懴埑價儞偺僷僢僉儞傪擖傟丄傆偨傪暵傔丄偟偭偐傝偲儁儞僠摍偱枾暵偡傞丅寖偟偔侾擔乮壞応丗20亷埲忋乯傕偟偔偼俀擔乮搤応丗10亷埲壓乯潣漚偡傞偙偲偱丄儂僗僎儞偺僿僉僒儞梟塼偑弌棃偨丅Triphosgene偼搶嫗壔惉偺傕偺傕梡偄偨偑丄Aldrich偺傎偆偑宍忬偑寢徎偱偁傝丄埖偄傗偡偐偭偨偺偱丄Aldrich傪偍慐傔偡傞丅
MOMBhc-chloroformate偺崌惉朄
婎幙偱偁傞MOMBhc-OH偲儂僗僎儞梟塼傪斀墳偝偣傞慜偵丄懴埑價儞拞偺埑傪壓偘傞丅幚嵺偺憖嶌偼斀墳30暘慜偵丄僨儏儚乕僼儔僗僐偵儊僞僲乕儖傪壛偊丄偦偙偵塼懱拏慺傪彊乆偵壛偊偰丄僈儔僗朹偱偐偒崿偤偨丅偁傞掱搙塼懱拏慺傪壛偊傞偲儊僞僲乕儖偑搥傝巒傔傞(-65亷)丅偦偙偵懴埑價儞傪擖傟丄30暘掱搙惷抲偟偨丅偦偺娫偵丄20 mL偺僫僗宆僼儔僗僐偵婎幙(3)傪161.2 mg (0.511 mmol)丄扙悈僩儖僄儞2 mL丄扙悈THF 2 mL傪壛偊丄傾儖僑儞僈僗暤埻婥壓侽亷偱奾漚偟偨丅30暘屻丄懴埑價儞傪奐偗丄僈儔僗僔儕儞僕偲僯乕僪儖傪巊偄丄慡偰偺儂僗僎儞偺僿僉僒儞梟塼傪拲堄怺偔僼儔僗僐偵擖傟傞丅廔傢偭偨傜偡偖偵丄傾儖僑儞僈僗暤埻婥壓偵偟偨丅TLC偱偺斀墳偺捛愓偼崲擄側偺偱丄NMR偵傛傞斀墳偺捛愓傪峴偭偨丅尨椏徚幐傪妋擣偟偨傜丄栺30暘娫傾僗僺儗乕僞乕偱儂僗僎儞僈僗傪幐妶偝偣偨丅梟攠傪尭埑彍嫀偟偨屻丄僿僉僒儞偲僋儘儘儂儖儉乮侾丗侾乯偺梟塼傪挷惢偟丄偦傟傪慹惗惉暔偵壛偊丄僗僺僫乕偱寖偟偔潣漚偟偨丅偦偟偰丄媧堷傠夁偟丄捑揳傪恀嬻壓偱姡憞偝偣傞偙偲偱丄栚揑暔傪170.3 mg (0.451 mmol, 88.2%)摼偨丅NMR偵傛傞斀墳捛愓偼侾帪娫偛偲偵應掕偡傞偺偑栚埨偱偁傞丅埲壓偵捛愓曽朄傪帵偡丅僷僗僣乕儖僺儁僢僩傪巊偄丄彮検 偺斀墳梟塼傪10 mL僫僗宆僼儔僗僐偵堏偟丄僋儘儘儂儖儉傪壛偊偰僺儁僢僩撪偺斀墳梟塼傪慡偰梟偐偟偨丅梟攠傪彍嫀偟丄廳僋儘儘儂儖儉偱NMR應掕傪峴偭偨丅
1H-NMR (270.05 MHz; CDCl3) 兟= 3.53 (3H, s), 5.33 (2H, s), 5.42 (2H, d, J=1.4 Hz), 6.43 (1H, s), 7.19 (1H, s), 7.64 (1H, s)
13C-NMR (67.80 MHz; CDCl3) 兟= 56.73, 67.08, 95.17, 104.19, 108.82, 111.77, 112.58, 127.27, 145.28, 150.62, 154.27, 156.74, 159.49
FT-IR (ATR) 兯= 1756, 1719, 1603, 1273, 1164, 1151, 943, 921, 897, 853
嶲峫暥專
丂
丂
偍栤偄崌傢偣丗搶朚戝妛棟妛晹惗暔暘巕壢妛壢丂屆揷庻徍
摉僒僀僩偺夋憸丒暥彂偺揮嵹傪堦愗嬛偠傑偡丅
Copyright© 2004丂Furuta lab Toho Univ.丂All Rights Reserved.
丂