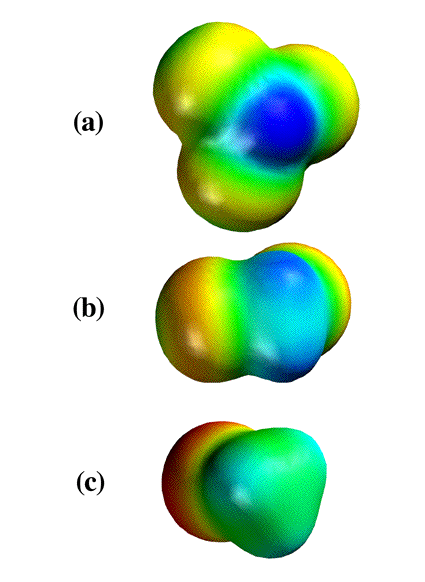1H NMR スペクトル(プロトン核磁気共鳴スペクトル)を“見て”理解しよう!
2)プロトン上の電子密度の違いによって化学シフトの違いを見る
大きな電気陰性度置換基がついた炭化水素では,置換基の電子吸引効果によって電子が電気引性度の大きな置換基に偏ります.そうするとその置換基がついている炭素上の水素の電子密度も低下します.
下の図は上からクロロホルム(a:CHCl3),ジクロロメタン(b:CH2Cl2),クロロメタン(c:CH3Cl)の静電ポテンシャルマップを示しています.
静電ポテンシャルマップとは,前のページで出てきた静電ポテンシャルの様子を分子の皮の上に地図のように色付けしたものです.電子に富んでいるところは赤く,電子に乏しいところは青くしてあります.
エネルギーの大きさと色の関係をそれぞれの分子で同じにしてやると,たとえばどの分子の水素が一番電子に乏しい水素なのかが色でわかります.
このようにして表示したクロロホルム,ジクロロメタン,クロロメタンを見ると,明らかにクロロホルムの水素が,いちばん濃い青となっており,次いでジクロロメタン,クロロメタンの順になっています.
これはクロロホルムのプロトンの周りの電子密度が三つの中でもっとも低く,次いでジクロロメタン,クロロメタンの順に電子密度が引くことを意味しています.
そのため,クロロホルムを外部磁場の中に入れた場合,メチンプロトンが感じる磁場は周りに電子のお布団をあまりかぶっていいないためそれほど弱められませんが,ジクロロメタン,クロロメタンではプロトンの周りに電子のお布団がクロロホルムよりも厚いために,それらのプロトンが感じる磁場は与えられている外部磁場より弱く感じて低い周波数側(高磁場側:スペクトルの右側)で共鳴することになります.